Pagina 1 di 2
Entropia
Inviato: 9 set 2009, 22:30
da Ippo
L'entropia è una funzione di stato. Considerando un tipico cilindro dotato di pistone che contiene N moli di un gas perfetto il cui indice adiabatico è
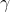
, possiamo scrivere l'entropia del gas in un modo che dipende solamente, diciamo, dal volume V e dalla temperatura T.
Si dimostri che si ha, a meno di una costante additiva,
=Nk_B \left( \ln (V) + {\ln (T) \over \gamma-1} \right))
Hint: usando fatti noti riguardo alle trasformazioni isoterme e adiabatiche si possono ottenere le relazioni tra
)
e
)
e tra
)
e
)
.
Viene dal Feynman, non è un esercizio molto "olimpico", ma mi è sembrato carino

Re: Entropia
Inviato: 10 set 2009, 16:44
da Pairo
Allora, vediamo se riesco;
parto dalla forma differenziale del primo principio della termodinamica:

.
e tenendo conto delle espressioni della energia interna e e del lavoro:

. Dividendo entrambi i membri per T:
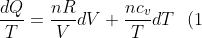)
e poiché si ha:

e

otteniamo il differenziale dell'entropia in funzione dei parametri richiesti. Integrandolo otteniamo l'espressione del testo, che è l'entropia a meno di costanti.
Re: Entropia
Inviato: 10 set 2009, 17:20
da Davide90
Direi proprio che vada bene.

(anche se varrà di più la conferma di Ippo)
Nell'ultima formula però volevi scrivere

infatti

,
e sostituendo quest'ultima espressione otteniamo la formula richesta dal problema.
Re: Entropia
Inviato: 10 set 2009, 17:46
da Ippo
esatto, Davide mi ha preceduto. Comunque ok, ormai Pairo è una garanzia

altro approccio - del tutto equivalente ovviamente:
il lavoro in un'espansione isoterma da
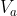
a
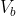
è notoriamente
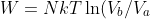)
, e la variazione di entropia, dato che siamo a temperatura costante, è
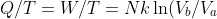)
(il calore è uguale al lavoro sempre perché siamo a temperatura costante). Allora
-S(V_a,T)=Nk \ln(V_b/V_a))
.
In un'espansione adiabatica invece si ha
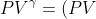V^{\gamma-1}=cost.)
da cui

e la variazione di entropia è nulla (non c'è scambio di calore), perciò si può scrivere, posto
}^{1 \over \gamma-1})
:
-S(V_a,T_a)=0)
-S(V_b,T_a) +S(V_b,T_a) -S(V_a,T_a)=0)
-S(V_b,T_a) +Nk\ln(V_b/V_a)=0)
-S(V_b,T_a)=-Nk\ln(V_b/V_a)=Nk\ln(V_a/V_b)=)
 \over \gamma-1})
Naturalmente
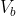
non ha nulla di speciale e possiamo sostituirlo con un V generico. Otteniamo infine
=S(1,T)+Nk \ln(V/1)=)
+Nk{\ln(T/1) \over \gamma-1}+Nk\ln(V/1)=)
+{\ln(T) \over \gamma-1} \right)+S(1,1))
da cui otteniamo che la costante additiva ignota dell'integrale di Pairo rappresenta l'entropia a volume e temperatura unitari per quel particolare gas. Feynman dice che questa cosa si chiama "costante chimica" e ha un particolare valore per ogni sostanza, determinabile empiricamente o con calcoli quantistici. Ganzo

Re: Entropia
Inviato: 10 set 2009, 18:56
da pascal
Ancora più semplice e compatta è la formula:
+costante)
Si vede che per un’adiabatica reversibile S=Costante.
Questa formula è contenuta anche nel problema n.6 dell’SNS 2001/2002
per chimici.
Re: Entropia
Inviato: 10 set 2009, 20:36
da Pairo
Sì, scusate refuso; grazie a Davide e a Ippo

. Comunque bella soluzione

Re: Entropia
Inviato: 10 set 2009, 21:08
da MrTeo
Ippo ha scritto:Feynman dice che questa cosa si chiama "costante chimica" e ha un particolare valore per ogni sostanza, determinabile empiricamente o con calcoli quantistici. Ganzo

Mi pare se ne parlasse anche nella termodinamica del Fermi, a partire dal teorema di Nernst (che del resto indica con 0 il valore di S di un cristallo puro a 0 K, quindi è già un riferimento)...

Re: Entropia
Inviato: 11 set 2009, 10:45
da Hope
eehm mi sono perso in questo passaggio oltre al V_b quale altre sostituzione sono state fatte per ottenere S(1,t) ed ln(V/1)?
Re: Entropia
Inviato: 11 set 2009, 11:03
da Ippo
Hope ha scritto:eehm mi sono perso in questo passaggio oltre al V_b quale altre sostituzione sono state fatte per ottenere S(1,t) ed ln(V/1)?
-S(1,T)=Nk\ln(V/1)=Nk\ln(V))
per quanto dimostrato sulle espansioni isoterme;
-S(1,1)=Nk{\ln(T/1) \over \gamma-1}=Nk{\ln(T) \over \gamma -1})
per quanto dimostrato con l'argomento sulle trasformazioni adiabatiche. In ogni equazione porti il termine negativo nell'altro membro ed ottieni esattamente quello sviluppo.

Re: Entropia
Inviato: 11 set 2009, 13:22
da Hope
grazie del chiarimento Ippo.
Ora propongo un esercizio un po piu semplice visto che siamo in tema di entropie e di dimostrazioni.
Due oggetti uguali con diversa temperatura T_1 e T_2 sono messi in una scatola dalle pareti adiabatiche e raggiungono l equilibrio termico.
dimostrare che l aumento di entropia in questo processo è
deltaS=\frac{2Q}{T_1-T_2}ln*\frac{(T_1+T_2)^2}{4T_1+T_2}
dove Q rappresenta il calore totale che passa dall oggetto caldo a quello freddo .
Supporre nella risoluzione che le loro capacità termiche siano indipendenti dalla temperatura.
Proviene dall'hallyday di meccanica dell università
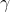 , possiamo scrivere l'entropia del gas in un modo che dipende solamente, diciamo, dal volume V e dalla temperatura T.
, possiamo scrivere l'entropia del gas in un modo che dipende solamente, diciamo, dal volume V e dalla temperatura T. =Nk_B \left( \ln (V) + {\ln (T) \over \gamma-1} \right))
) e
e ) e tra
e tra ) e
e ) .
.