Sì, scusate, mi sono sbagliato, grazie. Allora nel primo caso, l'errore porta ad una diversa espressione di
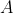
che corretta dovrebbe essere:
+C)}{nR})
Nel secondo caso, la temperatura diventa:
{T_0}}{nR+(n{c_V}+C)})
Passo al terzo punto. Riscriviamo il primo principio (questa volta con il segno giusto

):
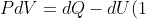)
Sostituendo,
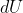
e tenendo conto che
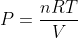
si ha:
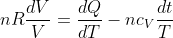
cioè
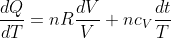
Possiamo ora integrare dallo stato iniziale allo stato finale, osservando che il membro di sinistra è proprio la variazione di entropia del sistema. Si ha:
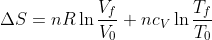
La variazione di entropia è allora determinata, poichè
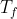
è stata calcolata nel punto 1, e
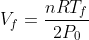
Per la variazione di entropia del secondo punto, ci accorgiamo che la trasformazione non è reversibile, ma poiché l'entropia del sistema è una funzione di stato, ne calcoliamo la variazione come al punto precedente, immaginando trasformazione reversibile tra gli stati iniziale e finale. Come prima, otteniamo perciò:
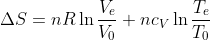
Dove
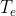
è quella calcolata al punto 2, e con
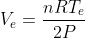
Per quanto riguarda l'entropia dell'universo: nel primo caso, si ha una trasformazione quasi statica, da cui la variazione di entropia dell'universo è
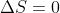
. Per il secondo caso ho invece qualche dubbio: poiché si tratta di una trasformazione irreversibile l'entropia dell'universo aumenta, ma ho difficoltà a rendere il tutto quantitativo.







 [/Intermezzo]
[/Intermezzo]