Vi chiedo un aiuto con questo problema:
Nella descrizione quantistica dell'atomo di H, per orbite circolari dell'elettrone, il momento angolare dell'elettrone rispetto al protone assume valori discreti di modulo pari a L=nh/(2pigreco), con h costante di Planck e n numero intero.
Applicando questa condizione a considerazioni di fisica classica, ricavare i possibili raggi e le possibili energie dell'elettrone in funzione di n, nota la sua carica e e la sua massa m.
Grazie in anticipo!!
Moto orbitale elettrone
Re: Moto orbitale elettrone
Conosciamo il suo momento angolare L da eguagliare con la sua espressione classima L=mvr, inoltre sappiamo che affincè l'elettrone sia in orbita la forza centrifuga eguaglia la forza di Coulomb. Metto tutto in un unico sistema per non perdere troppo tempo:
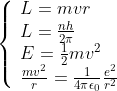
Da cui risolvendo (se non ho sbagliato i calcoli):

e

Da cui risolvendo (se non ho sbagliato i calcoli):
e
Re: Moto orbitale elettrone
grazie! ma per l'energia non c'è da tener conto dell'energia potenziale?
Re: Moto orbitale elettrone
Hai ragione, sono quegli errori stupidi che pur sapendo risolvere un problema te lo fanno sbagliare, L'energia potenziale èbohr ha scritto:grazie! ma per l'energia non c'è da tener conto dell'energia potenziale?
Re: Moto orbitale elettrone
ok... io mi ero incasinato considerando anche un'interazione gravitazionale che in questi casi va evidentemente trascurata... considerando la sola forza di coulomb e la potenziale elettrica è tutto più semplice! l'esercizio chiede anche un commento riguardo i risultati ottenuti: credi bastino considerazioni varie sulla quantizzazione dell'energia o aggiungeresti qualcosa di rilevante?
Re: Moto orbitale elettrone
N,o a parte che il raggio dell'orbita aumenta con il quadrato di n. Mi sono accorto però di qualcosa di strano: l'energia dell'elettrone è maggiore per orbite con n piccolo, questo è strano perchè le orbite di ordine superiore mi pare fossero più energetiche.
Re: Moto orbitale elettrone
Credo che si deve tener presente che l'energia di legame è NEGATIVA e inversamente proporzionale al quadrato di n, giacché per estrarre l'elettrone dobbiamo spendere lavoro dall'esterno. Per cui, per esempio, a n=1 corrisponde il valore più negativo e al crescere di n i valori si avvicinano sempre di più a 0 da sinistra. Ma, per dire, -1>-4! Forse intendevi questo: a valori più grandi di n corrisponde un valore relativo MAGGIORE ma un valore assoluto MINORE perchè l'elettrone in questi livelli è MENO legato.
Re: Moto orbitale elettrone
Scusate pe L'OT ma Bohr che chiede aiuto per la descizione quantistica dell'obitale dell'elettone e molto divertentebohr ha scritto:Vi chiedo un aiuto con questo problema:
Nella descrizione quantistica dell'atomo di H, per orbite circolari dell'elettrone, il momento angolare dell'elettrone rispetto al protone assume valori discreti di modulo pari a L=nh/(2pigreco), con h costante di Planck e n numero intero.
Applicando questa condizione a considerazioni di fisica classica, ricavare i possibili raggi e le possibili energie dell'elettrone in funzione di n, nota la sua carica e e la sua massa m.
Grazie in anticipo!!
