Pagina 1 di 1
Potenziale chimico.
Inviato: 1 apr 2011, 17:41
da Pigkappa
Consideriamo un recipiente in cui sono presenti particelle di 4 tipi, che chiamiamo

,
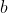
,

e
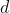
, che possono reagire come:

Sia
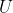
l'energia interna complessiva del contenuto del recipiente, e siano

,
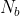
,

e

il numero di particelle di tipo

,
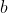
,

e
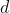
presenti.
Il potenziale chimico della specie

è definito da:

E in modo analogo sono definiti gli altri potenziali chimici.
Per capire di che si tratta, non ci importa più di tanto che si tratti di una derivata parziale e possiamo pensarlo semplicemente come

Provate a spiegare perchè, se la reazione è all'equilibrio, vale la relazione
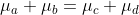
.
Re: Potenziale chimico.
Inviato: 26 mag 2011, 18:57
da Valenash
Proviamoci

Dato che hai scritto

suppongo che i coefficienti stechiometrici della reazione siano tutti 1, dunque

(essendo la reazione all'equilibrio, tot particelle di

reagiscono con le stesse particelle di
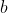
, e se ne formano altrettante di

e altrettante di
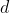
).
Dunque i denominatori son tutti uguali a meno del segno, infatti se da una parte si consumano, dall'altra si formano (poi torna indietro a ristabilire l'equilibrio), basta che sia verificato il bilancio energetico, (sempre coi segni scambiati).
E questo è vero, infatti tutta l'energia che liberano i reagenti trasformandosi in prodotti, sarà quella che (con segno opposto) viene restituita quando la reazione va in verso contrario, dunque è verificata l'uguaglianza.
Re: Potenziale chimico.
Inviato: 26 mag 2011, 21:05
da Pigkappa
Valenash ha scritto:basta che sia verificato il bilancio energetico, (sempre coi segni scambiati).
E questo è vero, infatti tutta l'energia che liberano i reagenti trasformandosi in prodotti, sarà quella che (con segno opposto) viene restituita quando la reazione va in verso contrario, dunque è verificata l'uguaglianza.
Ci stai andando vicino, ma non è proprio così. Nella definizione,
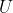
è l'energia interna. Non è detto che l'energia interna complessiva si conservi; parte dell'energia potrebbe andarsene in un altro modo (ad esempio in lavoro).
Non hai usato la condizione che avevo scritto:
se la reazione è all'equilibrio
Re: Potenziale chimico.
Inviato: 27 mag 2011, 18:12
da Valenash
Scusa, credo di essermi solo spiegato male =P
Comunque, noi sappiamo che la reazione è all'equilibrio, dunque se un po' di reagenti danno dei prodotti, poi questi tornano a reagire riformando i reagenti e mantenendo costante la K della reazione.
Ora, da questo possiamo dedurre che l'energia interna dei reagenti è uguale all'energia interna dei prodotti che si formano quando quei reagenti reagiscono.
Difatti, se non fosse così, la reazione diretta dovrebbe essere eso o endoenergetica, ma in ogni caso, quando la reazione si muove nel senso della liberazione di energia, questa si disperderebbe e (essendo la reazione inversa endoenergetica) i prodotti non potrebbero tornare a formare i reagenti, che va contro all'ipotesi che la reazione sia all'equilibrio.
Ora va meglio?? =)
Re: Potenziale chimico.
Inviato: 27 mag 2011, 21:30
da Pigkappa
L'hai spiegato un po' da chimico ma adesso va bene, è giusto. Io avrei detto che all'equilibrio l'energia interna complessiva è minima, e quindi per una reazione si ha
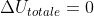
.
Questa relazione sui potenziali chimici è molto utile perchè, in certi casi, è possibile calcolare il potenziale chimico delle specie che costituiscono un sistema in funzione della temperatura, ed a partire da questa equazione si riesce ad ottenere la concentrazione delle varie specie. Il calcolo del potenziale chimico negli esempi che ho visto io è però troppo avanzato per questo livello (c'è anche dentro la costante di Planck...).
Re: Potenziale chimico.
Inviato: 28 mag 2011, 15:53
da Valenash
Pigkappa ha scritto:L'hai spiegato un po' da chimico ma adesso va bene, è giusto. Io avrei detto che all'equilibrio l'energia interna complessiva è minima, e quindi per una reazione si ha
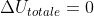
.
eheh lo so.. non a caso faccio un ITI ad indirizzo chimico =P
 ,
, 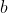 ,
,  e
e 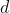 , che possono reagire come:
, che possono reagire come:
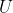 l'energia interna complessiva del contenuto del recipiente, e siano
l'energia interna complessiva del contenuto del recipiente, e siano  ,
, 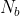 ,
,  e
e  il numero di particelle di tipo
il numero di particelle di tipo  ,
, 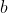 ,
,  e
e 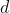 presenti.
presenti.  è definito da:
è definito da:

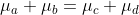 .
.