Pagina 1 di 1
Massimo lavoro estraibile
Inviato: 16 dic 2017, 13:44
da lance00
Si hanno due serbatoi contenenti entrambi
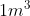
di acqua, il primo alla temperatura
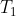
, il secondo alla temperatura
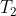
. Qual è il massimo lavoro estraibile da questo sistema?
Re: Massimo lavoro estraibile
Inviato: 17 dic 2017, 20:58
da JacopoTosca
Dato Q1 il calore tolto dal serbatoio 1 con temperatura T1 > T2, c = 4186 J / (Kg °C) e m = 1 Kg allora:
L= η Q1 e η = (T1 - T2)/ T2 e Q1 = c m (T1 - T2) , dato che rappresenta il calore sottratto all'acqua.
Unendo le equazioni risulta che L = (c m (T1 - T2)^2 )/T1
Re: Massimo lavoro estraibile
Inviato: 19 dic 2017, 18:37
da carol
Molto difficile e anch'io provo. Siccome la massima q di calore che può passare da
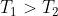
a
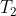
è quella ottenuta irreversibilmente miscelando le due acque che raggiungono alla fine la temperatura semisomma
/2)
, avevo pensato ad una serie di trasformazioni reversibili (cicli di Carnot) fra lo stesso stato iniziale e quello finale attraverso una macchina di Carnot ideale reversibile avente quindi il max rendimento per ogni ciclo che lavora fra la sorgente
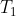
e il refrigerante
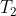
. Essa può lavorare estraendo calore alla sorgente e scaricandolo sul refrigerante finché le temperature di entrambi non si uguagliano nella semisomma
/2)
. Si può pensare ad una serie di cicli infinitesimi fra T (compreso fra la semisomma e
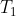
) e T'(il suo simmetrico rispetto alla semisomma compreso fra
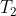
e la semisomma stessa). La macchina assorbe

a T e cede

a T' in modo che nel ciclo la variazione di entropia come in Carnot sia nulla e quindi il rapporto fra le q assorbita/ceduta è uguale a quello fra le temperature. Applicando lo scomponendo si ricava il lavoro
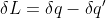
. Integrando per T che va dalla semisomma a
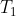
si trova il lavoro totale che dovrebbe essere il max possibile e che mi sarebbe venuto
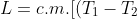 - (T_1 + T_2) log\frac{2T_1}{T_1+T_2}])
con c ed m calore specifico e massa del
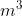
di acqua. Dimmi se può essere verosimile o se c'è qualche errore concettuale, della correttezza materiale dei calcoli ce ne importa poco!



Re: Massimo lavoro estraibile
Inviato: 19 dic 2017, 19:43
da lance00
carol la temperatura finale può essere minore di
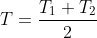
, pensaci bene

Re: Massimo lavoro estraibile
Inviato: 19 dic 2017, 19:51
da lance00
JacopoTosca: non puoi usare quella formula per il rendimento, le temperature dei due serbatoi man mano cambiano, non sono costanti
Re: Massimo lavoro estraibile
Inviato: 19 dic 2017, 22:15
da Gamow00
Chiamo la temperatura della sorgente calda
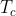
e quella della sorgente fredda
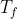
. La capacità termica di ognuna delle due masse d'acqua è
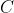
. Allora
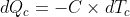
(il segno meno è dovuto dal fatto che il
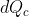
lo prendo positivo mentre
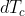
è negativo) e
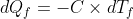
.Dividendo le due equazioni ottengo:
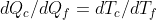
. Per massimizzare il lavoro lo scambio di calore deve avvenire grazie a una macchina di Carnot. Di conseguenza
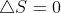
e
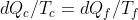
. Sostituendo nell'equazione sopra:
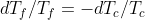
. Integrando ottengo:
=-ln(T_c)+cost)
. Quindi
=cost)
e di conseguenza
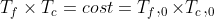
. Il calore smettera di fluire quando
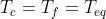
, quindi
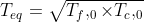
. Se il calore fosse fluito liberamente ( senza macchina di Carnot) la temperatura finale sarebbe stata
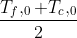
. Per calcolare il lavoro basterà calcolare l'energia termica che è stata persa, ossia
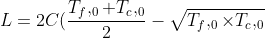)
Re: Massimo lavoro estraibile
Inviato: 20 dic 2017, 11:23
da carol
Re: Massimo lavoro estraibile
Inviato: 20 dic 2017, 18:35
da carol
Ci tengo a mostrare da casa con calma che anche il mio procedimento era giusto a parte la temperatura di equilibrio che anzichè dedurla dall'annullarsi della variazione d'entropia del ciclo avevo dato per scontato che dovesse essere la semisomma anzichè la media geometrica. Riprendendo il mio primo post abbiamo allora per l'annullarsi dell'entropia
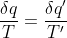
e applicando lo scomponendo si deduce subito

dove allora
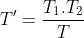
e quindi

.
Integrando si trova allora
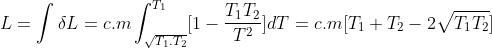
essendo c ed m rispettivamente il calore specifico e la massa del metro cubo di acqua.



Re: Massimo lavoro estraibile
Inviato: 20 dic 2017, 20:21
da JacopoTosca
lance00 ha scritto: ↑19 dic 2017, 19:51
JacopoTosca: non puoi usare quella formula per il rendimento, le temperature dei due serbatoi man mano cambiano, non sono costanti
Si hai ragione il sistema non è ideale. Mi ero reso conto dell'errore e stavo cercando una soluzione tramite gli integrali
Re: Massimo lavoro estraibile
Inviato: 21 dic 2017, 19:27
da lance00
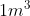 di acqua, il primo alla temperatura
di acqua, il primo alla temperatura 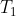 , il secondo alla temperatura
, il secondo alla temperatura 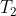 . Qual è il massimo lavoro estraibile da questo sistema?
. Qual è il massimo lavoro estraibile da questo sistema?