Due gas perfetti
Inviato: 1 giu 2016, 19:36
Un sistema termodinamico è costituito da un recipiente adiabatico immerso in aria a pressione atmosferica. Il recipiente è diviso in due parti A e B da una parete diatermica fissa e contiene nella parte A due moli di gas perfetto biatomico, nella B una mole di gas perfetto monoatomico. La parte A è chiusa da un pistone, la B da una parete mobile libera di scorrere senza attrito. Inizialmente i due sistemi sono in equilibrio termico alla temperatura 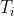 e il volume di A vale
e il volume di A vale  . Supponendo di espandere reversibilmente il gas A fino a raddoppiarne il volume, calcolare il rapporto tra
. Supponendo di espandere reversibilmente il gas A fino a raddoppiarne il volume, calcolare il rapporto tra  tra la temperatura finale ed iniziale del gas B.
tra la temperatura finale ed iniziale del gas B.
Se scrivo l'equazione di stato, trovo che la temperatura finale di A è il doppio, perché la pressione è costante. Ma anche quella di B deve essere il doppio, quindi il volume di B raddoppia... è possibile? Perché se scrivo invece il primo principio, mi verrebbe da pensare che invece B si comprime isobaricamente. Cosa sbaglio?
Se scrivo l'equazione di stato, trovo che la temperatura finale di A è il doppio, perché la pressione è costante. Ma anche quella di B deve essere il doppio, quindi il volume di B raddoppia... è possibile? Perché se scrivo invece il primo principio, mi verrebbe da pensare che invece B si comprime isobaricamente. Cosa sbaglio?