Pagina 1 di 6
Staffetta termodinamica
Inviato: 30 apr 2010, 22:33
da Gauss91
Ciao ragazzi. Penso che in questo thread non ci sia bisogno di premesse o di spiegazioni

.
Unica cosa: in "termodinamica" penso si includa anche la teoria cinetica dei gas.
Al mio segnale, scatenate l'inferno! Visto che siamo in termodinamica, ne avete ben donde!
 Problema 1
Problema 1 (Halliday): fare l'ipotesi [off topic]assurda, ma bisogna farla[/off topic] che la temperatura atmosferica T non vari con l'altezza. Dimostrare che, sotto quest'ipotesi, la pressione atmosferica varia con l'altezza y dal suolo secondo la legge
 = p_0 e^{-Mgy/RT})
, dove
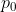
è la pressione al suolo e M è la massa molare dell'aria.
Re: Staffetta termodinamica
Inviato: 1 mag 2010, 20:30
da Rigel
Ci andiamo pesanti con le equazioni diferenziali

Re: Staffetta termodinamica
Inviato: 1 mag 2010, 21:01
da spn
Vabbè dai, ne ho visti di molto più calcolosi

.
Divido l'atmosfera in più strati, ognuno di altezza
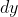
, in cui la pressione può considerarsi costante.
Fra uno strato e quello superiore, si ha
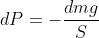
, dove dm è la massa dello strato superiore, e S la superficie delle basi degli strati, (si sta cosiderando che l'altezza rispetto al suolo non sia eccessivamente elevata, in modo che il campo gravitazionale sia costante).
Ora
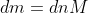
, ma considerando l'aria come un gas perfetto si ha:
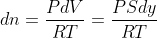
, da cui:
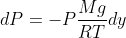
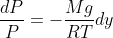
} {dP\over P}= - {M g \over R T} \int_{0}^{y} dy)
 \over P_0}=- {M g y \over R T})
 = P_0 e^{-M g y / R T})
Re: Staffetta termodinamica
Inviato: 1 mag 2010, 23:08
da spn
Visto che sono in voga le differenziali, vorrei proporre questo problema che secondo me è un sacco istruttivo; poi probabilmente esistono metodi diversi da quello che ho usato io:
Problema 2:
Un recipiente adiabatico chiuso contiene 5 moli di un gas perfetto monoatomico a pressione atmosferica, e un corpo di capacità termica
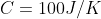
. Il volume del recipiente viene diminuito, finchè diventa la metà di quello iniziale. La trasformazione avviene lentamente, in modo che questa possa essere considerata reversibile e che il corpo abbia costantemente la stessa temperatura del gas. La variazione di volume del corpo interno è trascurabile. Trovare la pressione finale del gas.
Re: Staffetta termodinamica
Inviato: 2 mag 2010, 16:00
da .mg
@spn: giusto a livello formale, hai uguagliato due volte una quantità finita a una quantità infinitesima
Re: Staffetta termodinamica
Inviato: 2 mag 2010, 17:11
da spn
Già, purtoppo sui calcoli mi perdo molte formalità. Comunque modifico per i più precisi

.
Re: Staffetta termodinamica
Inviato: 2 mag 2010, 17:29
da .mg
Così va meglio

Se noti che
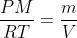
è la densità dell'aria allora hai
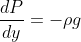
vale a dire la legge di Stevino in forma differenziale. Partendo da qui si fa un po' prima, ma il tuo ragionamento mi sembra che vada ugualmente bene

Re: Staffetta termodinamica
Inviato: 2 mag 2010, 20:42
da Ippo
Nota: il problema 1 è sostanzialmente il 3 della simulazione di Senigallia, senza le approssimazioni suggerite lì.
Re: Staffetta termodinamica
Inviato: 3 mag 2010, 19:54
da Rigel
Scusate se tolgo la possibilità di cimentarsi col problema ad altri baldi giovani

ma non ho resistito alla tentazione di risolvere questo quesito così carino

usando il primo principio della termodinamica modificato (o meglio la conservazione dell'energia) e il fatto che lo scambio di calore è nullo ho:

il calore scambiato con l'esterno ha il
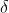
perchè non è un differenziale esatto (per saperne di più vi rimando all'Halliday

)
Inoltre da un pò di termologia so che
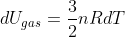
e
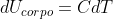
mentre usando la legge dei gas perfetti:
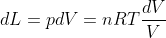
separando le variabili nella prima equazione e dividendo tutto per nRT, ottengo
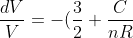\frac{dT}{T})
integrando
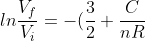ln\frac{T_f}{T_i})
e sostituendo i valori numerici (perdonatemi se vi risparmio i calcoli)
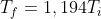
usando ancora la legge di stato dei gas perfetti ho
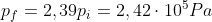
notare che l'equazione ricavata dopo l'integrazione non è altro che una versione modificato dell'equazione di Poisson (per temperatura e volume) per una trasformazione adiabatica. in questo caso l'esponente del volume dipende oltre che da
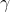
anche dalla capacità termica del corpo
Re: Staffetta termodinamica
Inviato: 3 mag 2010, 22:23
da spn

Il risultato dovrebbe essere corretto (almeno anche a me viene così). Come ha fatto notare Rigel, il metodo per risolverlo è sostanzialmente analogo a quello per dimostrare l'equazione per trasformazioni adiabatiche reversibili.
Vai col prossimo.
 .
.
 = p_0 e^{-Mgy/RT}) , dove
, dove 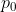 è la pressione al suolo e M è la massa molare dell'aria.
è la pressione al suolo e M è la massa molare dell'aria.