Trasformazioni termodinamiche
Inviato: 23 gen 2009, 21:11
Una mole di un gas perfetto monoatomico è portata da uno stato iniziale di pressione 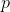 e volume
e volume 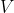 ad uno stato finale di pressione
ad uno stato finale di pressione  e volume
e volume 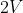 attraverso due processi diversi, entrambi reversibili:
attraverso due processi diversi, entrambi reversibili:
I) Prima si espande isotermicamente fino a raddoppiare il volume poi, a volume costante, si fa crescere la pressione fino al valore finale.
II) Si comprime dapprima isotermicamente finchè la pressione raddoppia e poi, a pressione costante, si lascia espandere fino al volume finale.
Calcolare per ciascun processo:
a) Il calore assorbito dal gas in ogni trasformazione.
b) Il lavoro fatto dal gas lungo ciascuna delle trasformazioni eseguite.
c) La variazione dell'energia interna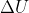
d) La variazione dell'entropia del gas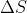
Tratto dall'Halliday
I) Prima si espande isotermicamente fino a raddoppiare il volume poi, a volume costante, si fa crescere la pressione fino al valore finale.
II) Si comprime dapprima isotermicamente finchè la pressione raddoppia e poi, a pressione costante, si lascia espandere fino al volume finale.
Calcolare per ciascun processo:
a) Il calore assorbito dal gas in ogni trasformazione.
b) Il lavoro fatto dal gas lungo ciascuna delle trasformazioni eseguite.
c) La variazione dell'energia interna
d) La variazione dell'entropia del gas
Tratto dall'Halliday