Soluzione numero 1: studio degli equilibri
Poniamoci nel sistema rotante con velocità angolare
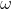
e consideriamo lo strado di gas sotteso da un piccolo angolo
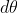
, compreso tra i raggi

e
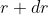
e di altezza
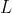
. Sulla superficie interna agisce la pressione
)
e quindi una forza
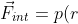Ld\theta \vec r)
, mentre sulla superficie esterna agisce la forza
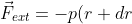Ld\theta (r+dr) \frac{\vec r}{r}=-(p(r)+p'(r)dr)Ld\theta (r+dr) \frac{\vec r}{r})
, inoltre la forza centrifuga è data da
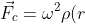 dV \vec r)
dove
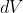
è l'elemento di volume
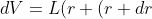)d\theta \frac{dr}{2})
e quindi
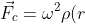L(2r+dr)d\theta \frac{dr}{2} \vec r)
.
Ora all'equilibrio si deve avere

e sostituendo le espressioni delle tre forze
rLd\theta+\omega^2 r\rho(r)L(2r+dr)d\theta \frac{dr}{2}=(p(r)+p'(r)dr)Ld\theta (r+dr))
, semplificando e trascurando i termini
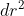
rispetto a quelli
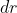
si ottiene l'equzione
=p(r)+r p'(r))
.
Ora serve una relazione tra pressione e densità, usando quindi l'equazione di stato dei gas perfetti e chiamando con
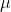
la massa molare si ottiene
=\rho (r) \frac{RT}{\mu}=a\rho(r))
dove

, sostituendo si ottiene l'equazione differenziale per la densità:
=\rho(r)(\omega^2 r^2-a))
Che è una bella equazione a variabili separabili che ha la bella soluzione:
= C \frac{\displaystyle e^{\frac{m \omega^2 r^2}{2K_bT}}}{r})
(dove m è la massa di una particella)
che sembra non avere nulla di male se non fosse per il fatto che se tentiamo di trovare la costante di integrazione ci tocca di integrare
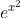
di cui non si ha una forma esplicita.
Vediamo ora se torna usando l'altro metodo.
Soluzione numero 2: distribuzione di Boltzmann
La distribuzione di Boltzmann afferma che in un sistema termodinamico a temperatura costante il numero di particelle che si trovano nella zona a potenziale

è proporzionale a
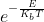
.
Ora notiamo che nel nostro sistema le zone con lo stesso potenziale sono i gusci cilindrici di altezze
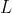
raggi

spessori
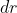
e se li la densità vale
)
nel guscio avremo
)
particelle date da
=\frac{\rho(r) 2\pi r L }{m}dr)
mentre il potenziale della particella nel guscio è il potenziale centrifugo

.
Dunque utilizzando la distibuzione di Boltzmann sappiamo che
}=costante)
e da qui si ricava:
= C \frac{\displaystyle e^{\frac{m \omega^2 r^2}{2K_bT}}}{r})
che è la stessa di prima, e visto che torna con i due metodi il sospetto che è corretta inizia a salire...