Pagina 3 di 4
Re: 85. Sistema termodinamico
Inviato: 25 lug 2016, 23:41
da FedericoC.
Sono d'accordo su quanto hai detto, ma noi per trasferire calore da uno scompartimento all'altro supponiamo di servirci di una macchina termica per la quale la parte 2 sarà il serbatoio caldo mentre la parte 1 quello freddo. Ora noi sappiamo che tra tutte le macchine termiche quella con rendimento maggiore è quella di Carnot che opera in modo reversibile. Ora considerando infinitesimi cicli tra le temperature istantanee dei due serbatoi si arriverà all'equilibrio termico. Dato che il calore sottratto al serbatoio caldo è il medesimo da qualsiasi macchina termica quella con rendimento maggiore sarà quella che estrae maggior lavoro dal sistema, dato che

. Dato che si sono utilizzati cicli infinitesimi reversibili la variazione di entropia sarà comunque nulla.
Re: 85. Sistema termodinamico
Inviato: 26 lug 2016, 17:45
da rocco
Non voglio dare l'impressione di voler polemizzare o voler avere l'ultima parola. Il procedere per cicli infinitesimi non può oscurare il dato di fatto che lo stato finale è

da quello iniziale e quindi la funzione di stato deve essere diversa nei due stati. Tu stesso nella tua espressione del lavoro e dell'entropia usi t.fin che è diversa da quelle iniziali dei due gas. Un ciclo infinitesimo torna comunque da dove parte sennò non è un ciclo. Poi non riesco a capire dove possa essere sbagliato massimizzare il lavoro con una temperatura finale che rientra fra quelle possibili del sistema. Quindi propongo di tenere ognuno le proprie convinzioni sperando che intervenga qualche lume.
Re: 85. Sistema termodinamico
Inviato: 26 lug 2016, 23:21
da step98
Per avere una variazione di entropia nulla il sistema non deve per forza ritornare nello stato di partenza, anzi in un sistema isolato che compie solo trasformazioni reversibili si ha sempre una variazione di entropia nulla (é maggiore di zero invece se il sistema isolato compie anche trasformazioni irreversibili). Nel nostro caso i due gas e la macchina termica che opera tra di essi costituiscono un sistema isolato che compie solo trasformazioni reversibili, quindi la variazione di entropia deve essere nulla. Secondo me l'errore nel tuo ragionamento sta nel fatto che consideri la temperatura
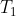
una temperatura finale possibile per il sistema, ma non essendo in questo caso la variazione di entropia nulla, ci sarebbe una violazione del secondo principio della termodinamica.
Re: 85. Sistema termodinamico
Inviato: 27 lug 2016, 18:24
da rocco
Siamo d'accordo ad arrivare alla stessa espressione del lavoro in funzione della temperatura finale: dov'è l'errore se essa viene massimizzata a
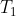
? Tu dici perchè non la può raggiungere in quanto la variazione di entropia deve essre nulla perchè si tratta di trasformazioni reversibili. E' un pò il gatto che si mangia la coda...
E poi c'è un dato grosso come una casa: io do un risultato, Federico non è in grado di darlo(dice per motivi tecnici): ma il testo è chiarissimo al riguardo. Bisogna determinare il massimo lavoro estraibile. Quindi il libro da cui ha preso il testo darà pure il risultato!

Lui dice che da la stessa soluzione. Ma qual'è il risultato? Lo dia e siamo a posto

Re: 85. Sistema termodinamico
Inviato: 27 lug 2016, 19:32
da FedericoC.
Non ho mai detto di non avere un risultato, anzi te lo posto subito

, ho preferito dare il procedimento che credo sia la parte più importante e istruttiva di un problema di fisica, bastava fare i calcoli..
Re: 85. Sistema termodinamico
Inviato: 28 lug 2016, 18:01
da rocco
Grazie, finalmente. Ci studierò immaginando che sia anche il risultato del libro. Ho continuato intanto a riflettere e sento il bisogno della tua critica per queste riflessioni (se vorrai)perchè quasi certamente le hai già effettuate e ti ringrazio in anticipo. Credo che sia assodato
1) che qualunque trasformazione subiscano i due gas debba essere adiabatica perchè sono isolati dall'esterno e fra loro
2) il problema è se sia reversibile o no, a variazione nulla di entropia oppure no.
3) è qui che mi tornerebbe di mettere che sia reversibile per ottenere il lavoro massimo, perchè siamo solo nell'ambito delle ADIABATICHE e non di tutte le trasformazioni (infatti ti dissi, e tu ti dicesti d'accordo, che l'adiabatica fra due stati non aveva il lavoro massimo perchè si può trovare un'isobara ed un'isovolumica reversibili a lavoro maggiore fra gli stessi stati)
4) ed ecco il grande dubbio: la relazione che dà il nostro lavoro è fondata su L=

ovvero su

ovvero sul primo principio che riguarda tutte le trasformazioni; ma se deve essere adiabatica reversibile deve essere

ovvero

. Perchè dal primo principio non discende questo automaticamente? Mi puoi chiarire perchè se il numeratore è nullo non si annulla anche la frazione?
Evidentemente non sta così perchè altrimenti non avresti bisogno di trovare
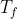
....
Re: 85. Sistema termodinamico
Inviato: 28 lug 2016, 21:12
da FedericoC.
Ti rispondo molto volentieri

Innanzi tutto anche se l'entropia è una funzione di stato non è detto che affinchè la sua variazione sia nulla il sistema debba essere nello stesso stato, sarebbe come dire che per avere una variazione nulla di temperatura o pressione il sistema debba essere invariato e questo ovviamente non è necessario. Questo per chiarire il problema che avevi posto e a cui non avevo ancora risposto.
Poi a dire il vero non penso che le trasformazioni cui sono sottoposti i due gas possano essere solo adiabatiche. Consideriamo lo scomparto 2, quello caldo, la macchina termica estrae da questo del calore
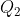
quindi il calore per questo singolo setto non è nullo e quindi la trasformazione cui è stato sottoposto non adiabatica. Essendo una macchina termica da questo calore estrae del lavoro, per poi cedere del calore
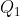
minore di
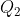
allo scomparto 1, quindi anche per quest'ultimo il calore non è nullo e la trasformazione non adiabatica. Secondo me l'utilizzo che hai fatto del primo principio seppure corretto è "inusuale" e trae un po' in inganno. Il lavoro che noi vogliamo trovare non è quello direttamente compiuto dai gas come quello per spostare il setto isolante, ma quello estratto dal sistema da una macchina termica. Ora dato che il lavoro compiuto da ogni scomparto e opposto all'altro il lavoro totale che il sistema compie considerando entrambi gli scomparti è nullo, quindi la variazione di energia interna corrisponde anche allo scarto di calore che la macchina termica ha tramutato in lavoro, cioè

. Spero di essermi spiegato bene in questo passaggio che forse è quello chiave.
Sta di fatto che comunque la relazione che tu proponi per il lavoro è corretta e anche il massimizzarla per
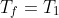
è assolutamente ragionevole, tuttavia penso come Stefano che l'errore stia nel considerare quella temperatura come effettivamente possibile, come temperaura finale, per il nostro sistema, non si può sapere a prescindere se non viola il secondo principio della termodinamica e in questo caso penso proprio lo faccia.
Spero di essermi spiegato in modo comprensibile, se qualcosa non è corretto o chiaro dimmi pure

Re: 85. Sistema termodinamico
Inviato: 28 lug 2016, 22:34
da step98
Perfettamente d'accordo con quello che ha scritto Federico, preciso solo che parlavo di sistema isolato perché la trasformazione dell'intero sistema è adiabatica, e non quelle dei singoli scompartimenti, che come ha fatto notare Federico non lo sono affatto perché c'è la macchina termica che assorbe calore da uno scompartimento e lo cede all'altro.
Re: 85. Sistema termodinamico
Inviato: 29 lug 2016, 17:17
da rocco
E' incredibile ma più discutiamo e meno siamo d'accordo: per il primo punto non è calzante l'esempio della temperatura e della pressione giusto perchè esse non sono funzioni di stato! Ti prego di farmi un esempio, che non sia il caso dell'adiabatica reversibile!, in cui stati diversi di un certo sistema hanno la stessa entropia. Secondo me è una contraddizione in termini che una funzione di stato non dipenda dallo stato a meno che non sia previsto (adiabatica reversibile) che sia costante in tutti gli stati.
Poi l'altro aspetto per me misterioso: ma dov'è la macchina termica? Che preleva il calore da un gas (che è TERMICAMENTE ISOLATO da tutto) e lo trasferisce all'altro (che è ancora TERMICAMENTE ISOLATO da tutto). Il testo parla di un recipiente diviso in due comparti isolati fra loro e dall'esterno. Dov'è il fluido termodinamico, di Carnot per es., che si sposta da una sorgente ad un'altra prelevando calore dall'unica base di un termostato che non è isolante e cedendolo all'altra attraverso la base non isolante? Infatti per realizzare l'adiabatica si pone il fluido di Carnot su base isolante come sono i contorni di ciascun gas nel nostro caso.
Nella nostra circostanza l'unica cosa mobile (macchina?)è il setto scorrevole che si muove sulla base della differenza di pressione.
Sono scoraggiato perchè evidentemente io non vedo cose che voi vedete (a meno che non le suggerisca il libro da cui hai preso il testo). Con che coraggio posso provare il test SNS? Bianciardi in Problemi di fisica dice che non bisogna mai arrendersi...
Re: 85. Sistema termodinamico
Inviato: 29 lug 2016, 20:16
da FedericoC.
Mi dispiace contraddirti, ma temperatura e pressione SONO funzioni di stato, puoi avere un rapido riscontro cercando su internet "funzioni di stato", quindi credo che l'esempio portato possa essere calzante. Detto ciò penso possa essere assodato che non serve che il sistemi sia nello stesso stato iniziale affinchè la variazione di entropia sia nulla.
In secondo luogo il testo del problema non da alcun suggerimento, l'idea della macchina termica dovrebbe venire poichè altrimenti come si potrebbe estrarre lavoro dal sistema? Il lavoro compiuto dai due gas è complessivamente nullo poichè
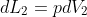
mentre
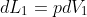
e
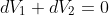
.
Ad ogni modo non credo tu debba scoraggiarti solo per questo problema, chiedi pure se qualcosa ancora non va

 . Dato che si sono utilizzati cicli infinitesimi reversibili la variazione di entropia sarà comunque nulla.
. Dato che si sono utilizzati cicli infinitesimi reversibili la variazione di entropia sarà comunque nulla.