Pagina 2 di 4
Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 0:41
da FedericoC.
Antonio, dalla forma del risultato direi che il ragionamento e il procedimento sono corretti, se non sbaglio hai fatto un errore di calcolo nel trovare la temperatura finale, ad ogni modo direi di postare i procedimenti

Per Poor, l'errore nel ragionamento sta nel considerare il calore nullo, bisogna immaginare di prelevare del calore dal serbatoio caldo e trasferirne una porzione a quello freddo...
Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 2:19
da Antonio Mele
PRIMO PUNTO:
I due gas per stare all'equilibrio devono avere la stessa pressione. Quindi riesco a ricavarmi i volumi iniziali dei due gas mettendo a sistema l'equazione di stato dei gas perfetti tenendo conto che la pressione è uguale e che

.
SECONDO PUNTO
Per calcolare il massimo lavoro estraibile ho pensato un po' al massimo lavoro che può svolgere una macchina termica con trasformazioni reversibili.
Se immaginiamo come per magia che il calore venga prelevato dalla sorgente più calda e immesso in quella più fredda senza che quest'ultimo attraversi il pannello isolante, la temperatura all'intero dei due gas cambia e di conseguenza anche il volume e la pressione. Il lavoro massimo che si ottiene sarebbe quello speso per far muovere il pannello isolante. Il gas a cui è stato ceduto calore si espande mentre l'altro si comprime fino a raggiungere entrambi la stessa temperatura
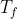
e lo stesso volume

.

Usando il primo principio della termodinamica mi trovo facilmente a quanto corrispondono
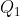
e
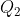
, dopodichè vado a sostituire nella precedente equazione con l'accorgimento che

. Ora per calcolarmi il lavoro mi manca solo la temperatura finale da trovarmi. Me la posso facilmente ricavare ponendo la variazione di entropia totale (la somma tra le due variazioni) uguale a 0 e posso farlo visto che abbiamo supposto che la trasformazione sia reversibile.
TERZO PUNTO.
La temperatura finale me la trovo ponendo

.
La variazione di entropia sarebbe la somma tra le variazioni di entropia relative ai due gas.
L'unico accorgimento da fare è quello che il volume finale per entrambi i gas sarebbe la metà del volume totale.
Se c'è bisogno di scrivere tutti i vari passi in formule, lo faccio, ma è una tortura scrivere tutti quei logaritmi!
Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 10:00
da FedericoC.
Tutti i procedimenti sono perfetti e spiegati bene! Direi di consegnarti il testimone della staffetta senza perderci in calcoli

Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 11:18
da rocco
FedericoC. ha scritto:
Per Poor, l'errore nel ragionamento sta nel considerare il calore nullo, bisogna immaginare di prelevare del calore dal serbatoio caldo e trasferirne una porzione a quello freddo...
Scusa se mi sostituisco a poor ma ho seguito il suo ragionamento e, per amor di verità, credo che sia giusto. Il calore nullo si riferisce infatti allo
scambio con l'esterno e il recipiente è isolante: pertanto il lavoro estraibile deve proprio essere la max variazione di energia interna cambiata di segno per il primo principio. Ma questa si ha proprio quando 2 cede calore ed 1 non lo assorbe rendendolo disponibile per il lavoro. Infatti
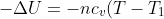-nc_v(T-T_2))
con T temperatura finale. Si vede subito che essa è max, e quindi L è max, quando
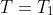
in cui il primo termine, che sarebbe negativo, si annulla e il secondo termine, che sarebbe positivo, è massimo. Mele dovrebbe dare il risultato invece delle formule e vediamo se è diverso da questo.
Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 11:35
da FedericoC.
Se io prelevo del calore
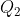
dal serbatoio più caldo e si fornisce del calore
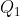
a quello più freddo ottengo del lavoro che per la conservazione dell'energia deve essere
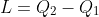
. Se applichiamo il primo principio della termodinamica a ciascuno dei due scomparti che sono sistemi isolati in quanto tutte le pareti incluso il setto sono isolanti otteniamo
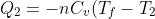-PdV_2)
e
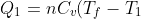+PdV_1)
. Da qui possiamo ricavare il lavoro che è massimo quando tutte le trasformazioni sono reversibili cioè quano la variazione di entropia è nulla.
La relazione che hai scritto infatti è corretta ed è alla fine se si ordina
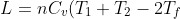)
, cioè quello che si ottiene col ragionamento fatto sopra, ma non è coretto dire che il massimo si ha per
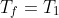
.
Scusate se prima non sono stato chiaro, non avevo capito bene cosa si intendeva per calore nullo, perchè io avevo considerato due sistemi anzichè uno unico..

Ad ogni modo provate se vi va a trovare la temperatura finale, il testimone va comunque ad Antonio che ha fatto correttamente i primi due punti

Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 17:01
da rocco
FedericoC. ha scritto:.
La relazione che hai scritto infatti è corretta ed è alla fine se si ordina
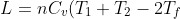)
, cioè quello che si ottiene col ragionamento fatto sopra, ma non è coretto dire che il massimo si ha per
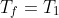
.
Scusami davvero se sono un rompiscatole e sai bene che non c'entra la questione del testimone a Mele. Ma devo capire: se la mia relazione è corretta come dici per farla coincidere con la tua dovrebbe essere
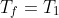
nella tua? Grazie e scusa ancora ma si impara così...
Re: 85. Sistema termodinamico
Inviato: 24 lug 2016, 17:41
da FedericoC.
Figurati si fa sempre bene a chiedere e chiarire confrontandosi anche perchè tutti sbagliano e magari ho sbagliato io.
La relazione cui siamo arrivati per il lavoro è la medesima cioè
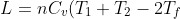)
che è una semplice riscrittura della tua variazione di energia interna cambiata di segno. Ora data questa relazione il problema chiede quale sia il massimo lavoro estraibile dal sistema alias la temperatura finale
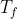
cui questo avviene, ora tu dici che si ha per
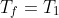
ed è qui che secondo me non è corretto. Il massimo lavoro si ha quando si opera in modo reversibile quindi quando la variazione di entropia è nulla.
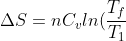+nRln(\frac{V}{2V_1})+nC_vln(\frac{T_f}{T_2})+nRln(\frac{V}{2V_2}))
Usando la legge dei gas perfetti per sostituire ai volumi un'espressione in funzione della temperatura si arriva infine a:
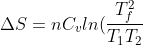+nRln(\frac{(T_1+T_2)^2}{4T_1T_2}))
Ora ponendo
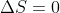
si potrebbe trovare
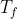
che è una cosa un po' brutta ma che volendo posso scrivere, ad ogni modo a noi interessa più che altro verificare se
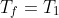
sia soluzione, sostituendo risulterebbe:
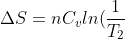+nRln(\frac{(T_1+T_2)^2}{4T_1T_2}))
che se non ho sbagliato calcoli non fa zero
Spero di essere stato chiaro in caso qualcosa non funzioni dimmi pure

Re: 85. Sistema termodinamico
Inviato: 25 lug 2016, 18:31
da rocco
Mi dispiace insistere: noi abbiamo e siamo concordi una espressione del lavoro in funzione della temperatura finale. Essa può essere una qualunque fra la minima e la massima del sistema cioè

. Qual è quella che massimizza L come chiede il testo? Quella che minimizza il sattraendo

ovvero
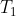
e dunque il mio risultato è
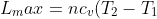)
ovvero quella che realizza la massima diminuzione di energia interna del sistema: quella di 1 rimane al minimo, quella di 2 diminuisce della maggiore quantità possibile. Riguardo al tuo discorso sull'entropia è un terreno scivoloso perchè è difficile stabilire la corrispondente reversibile che porta dallo stesso stato iniziale allo stesso stato finale. Visto che i due argomenti del log non possono essere 1 (sennò nel secondo dovrebbe essere
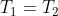
) per trovare
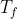
occorre un calcolo che mi pare improbabile sia richiesto. Mentre nel mio caso è indiscutibile che il lavoro si massimizza per quel valore e ad occhio mi pare più verosimile come soluzione che è fondata sul primo principio e non c' è possibilità di sbagliare come nella scelta della reversibile.
Re: 85. Sistema termodinamico
Inviato: 25 lug 2016, 19:43
da FedericoC.
Mi dispiace di non saperti rispondere in modo più convincente, magari qualcun'altro saprà farlo. Ad ogni modo la soluzione che ti ho proposto con il secondo principio della termodinamica è lo stesso dato dalla soluzione del testo (ciò non toglie che possa essere sbagliata). Personalmente io ho optato per questo procedimento ispirato dal problema di Senigallia di termodinamica di quest'anno

Re: 85. Sistema termodinamico
Inviato: 25 lug 2016, 21:53
da rocco
FedericoC. ha scritto: Il massimo lavoro si ha quando si opera in modo reversibile quindi quando la variazione di entropia è nulla.
Spero di essere stato chiaro in caso qualcosa non funzioni dimmi pure

Credo proprio che questo ragionamento sia sbagliato. La reversibilità non implica una variazione nulla di entropia come tu sostieni a meno che non si tratti di un CICLO (e non è il nostro caso) poichè l'entropia è funzione di stato. E' inutile che ti faccia esempi, che conosci benissimo, di reversibili non cicliche (con stato iniziale DIVERSO da quello finale come nel nostro caso) in cui la variazione d'entropia è diversa da 0 e quindi è inutile che tu ricerchi quello stato finale per cui la variazione è nulla. Dovrebbe coincidere con lo stato iniziale. Certo si può pensare all'adiabatica reversibile ma non è certo a lavoro massimo: se prendi un'adiabatica reversibile fra due stati si può trovare un'isobara e un'isovolumica fra gli stessi stati a lavoro maggiore...Quindi io non so cosa dire del testo di cui parli e son pronto a riconoscere un mio eventuale abbaglio...ci mancherebbe...ma credo non sulla base della tua argomentazione che ho citato. Staremo a vedere eventuali novità.
